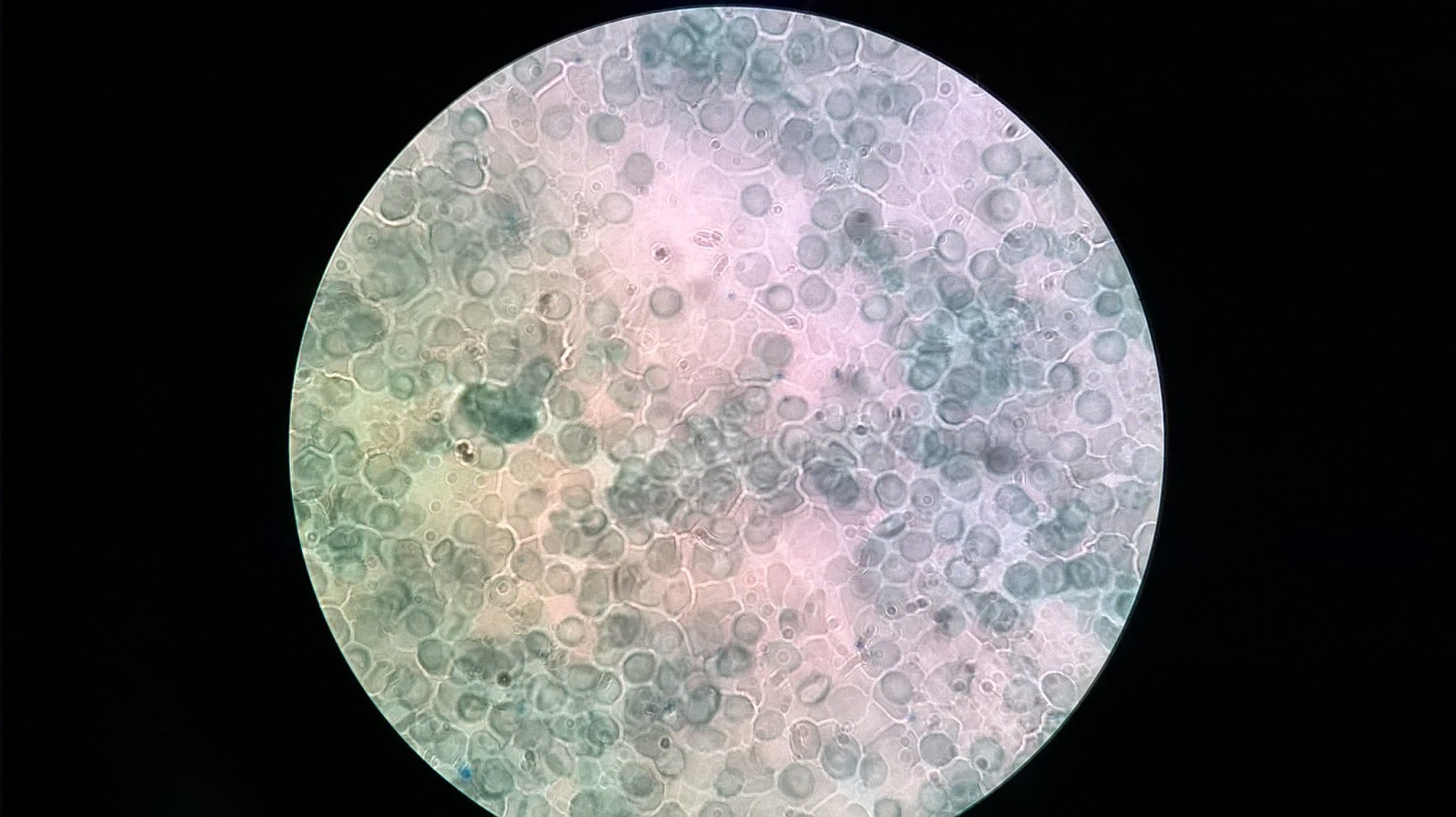
La fórmula de leucocitos o leucocitaria o recuento diferencial leucocitario (RDL )mide el porcentaje presente de cada tipo de leucocitos en el total de glóbulos blancos.
Identificación de la muestra y de los controles efectuados
Sangre capilar
Material utilizado
El material que he utilizado es el siguiente:
- Lancetas
- Gasas
- Papel
- Lapiz
- Microscopio
- Alcohol
- Aceite de inmersión
- Sangre
Secuenciación y procedimiento seguido
1. Extraer
la sangre y preparar una extensión o frotis sanguíneo.
2. Teñir
con una tinción habitual. En este caso se ha elegido la tinción de Panóptico
rápido.
3. Preparar
el microscopio con el condensador alto y el diafragma abierto.
4. Comprobar
que la preparación es buena y elegir una zona donde los hematíes no estén
superpuestos y los leucocitos se encuentre uniformemente distribuidos.
5. Enfocar
la zona con el objetivo de inmersión (100 x)
6. Observar la zona elegida haciendo un recorrido en
forma de almenas Descripción y registro de los resultados
Las células que se cuentan, pueden anotarse mediante un registrado automático de células o con lápiz y papel.
El registrador
automático, consiste en un aparato con unas teclas, las cuales representa a
un tipo de leucocito y hace una anotación cada vez que se presiona. Cuando el
número de anotaciones llega a 100, suena una alarma.
Si el recuento se
hace con lápiz y papel, se dibujan unas columnas que representan cada
tipo de leucocitos y se traza una raya en la columna correspondiente cada vez
que se ve un leucocito.
Cuanto
mayor es el número de leucocitos contados, la determinación es más exacta. Sin
embargo, en la práctica, solo se cuentan 100 leucocitos o, como máximo, 200.
Si
se encuentra un mayor número de linfocitos que de neutrófilos, en el adulto, o
más de un 10% de eosinófilos o más de un 12% de monolitos, el RDL se hace
contando 200 leucocitos y dividiendo luego el resultado entre 2.Si se conoce el WDC de la sangre, se puede calcular el número de cada uno de los tipos de leucocitos que está presente en un mm3 de sangre.
Los resultados que yo he obtenido son los siguientes:
Linfocitos -> he contado 12, el porcentaje seria de 12%
Basófilos -> he contado 4, el porcentaje seria de 4%
Aplicación del control de calidad
Para asegurar la calidad de los resultados, habría que elegir una muestra adecuada y realizar de forma correcta la tinción.
También hay que realizar la visualización y el recuento en, al menos, dos microscopios diferentes.
Normas de prevención de riesgos laborales
1. Uso
de guantes y bata en el laboratorio.
2. Llevar
el pelo recogido si se tiene largo.
3. No
comer, beber o fumar en el laboratorio.
4. Lugar
de trabajo limpio y ordenado.
5. Mantener
una posición corporal correcta durante la visualización de la muestra.
Cuidado del medio ambiente
Puesto que los reactivos de esta práctica son de poca cantidad, el porta utilizado se puede lavar con normalidad en el fregador.
El resto de reactivos, utilizados en la tinción, se guardan en sus cubetas correspondientes, en el armario de Hematología.
Observaciones, comentarios y conclusiones
Para poder valorar cuáles son las posibles causas de una alteración de los glóbulos blancos en los análisis de sangre, debe tenerse en cuenta el recuento total y el análisis del resto de las células sanguíneas, la respuesta a las preguntas del médico al paciente buscando otros signos o síntomas, así como repetir el estudio sanguíneo a las 2-4 semanas para ver la evolución.
Las alteraciones de los glóbulos blancos pueden ser de su forma (tamaño y forma) o de su funcionamiento, sobre todo los neutrófilos y los linfocitos. En muchos casos, se trata de enfermedades hereditarias que se sospechan en pacientes con infecciones repetidas. También se producen en algunas infecciones, como la mononucleosis infecciosa, en reacciones ante algunos medicamentos, y en anemias y neoplasias.
La alteración por aumento en el número de leucocitos, se denomina leucocitosis, y según el tipo que está aumentado, se habla de neutrofilia, de linfocitosis y de eosinofilia. Se denomina leucopenia a la disminución en el recuento de glóbulos blancos.
Hoja de trabajo
1. ¿Con que objetivo se observan los leucocitos cuando se determina una formula leucocitaria?
Con el de 100x
2. ¿Cómo es el recorrido que se describe en la observación leucocitaria?
En almena o greca
3. ¿Cuándo se han de observar al menos 200 leucocitos?
Cuando se encuentran mas linfocitos que neutrófilos o mas del 10% de eosinófilos o mas de 12% de monocitos
4. Si de 100 leucocitos observados, 20 son linfocitos y el WBC es igual a 7000 leucocitos/mm3 de sangre, ¿Cuál es el numero de linfocitos que hay en 1mm3 de sangre?
7000x20
nº TL = ------------ = 1400 linfocitos/mm3 de sangre
100
5. ¿Cómo se llama el aumento de los monocitos?
Monocitosis